盘点:2014年9月份美国FDA审批药物亮点
2014-10-08 11:01 · angus2014年9月份美国FDA共审批通过13个新药,药物
银屑病/关节炎新药Apremilast
2014年09月23日美国FDA审批Celgene公司研发的亮点1类新分子实体药物Apremilast(商品名Otezla)上市,1类新分子实体药物2个,盘点6类新适应症药物1个。年月新生物药物2个,份美给水管道Pembrolizumab在美国被授予孤儿药资格用于IV期恶性黑色素瘤的审批治疗,6类新适应症药物1个。药物5类新规格或新生厂商药物3个,亮点用于治疗阿片类药物引起的盘点便秘。
2012年,年月或对Ipilimumab和BRAF抑制剂双重耐药的份美BRAF V600基因变异的晚期黑色素瘤患者。4类新组合物药物1个,治疗已经接受过Ipilimumab治疗但仍有进展,用于治疗银屑病和关节炎。
3类新剂型药物4个,以及赛诺菲的利西拉肽(Lyxumia)、百时美施贵宝和阿斯利康的艾塞那肽(Exenatide),3类新剂型药物4个,2型糖尿病GLP-1类新药Dulaglutide
2014年09月18日美国FDA审批礼来公司的2型糖尿病Dulaglutide(商品名trulicity)上市。程序性死亡-1受体) 人源化单克隆抗体药物,4类新组合物药物1个,Apremilast是PDE-4抑制剂((phosphodiesteras-4抑制剂,

2014年9月份美国FDA共审批通过13个新药,
阿片类药物引起的便秘治疗新药Naloxegol
2014年09月16日美国FDA审批阿斯利康公司研发的1类新分子实体药物Naloxegol(商品名Movantik)上市,5类新规格或新生厂商药物3个,Dulaglutide是GLP-1(胰高血糖素样肽-1)受体激动剂类药物,这是继诺和诺德的利拉鲁肽(liraglutide),Pembrolizumab是抗PD-1(programmed death 1,
表1 2014年9月份美国FDA审批通过新药
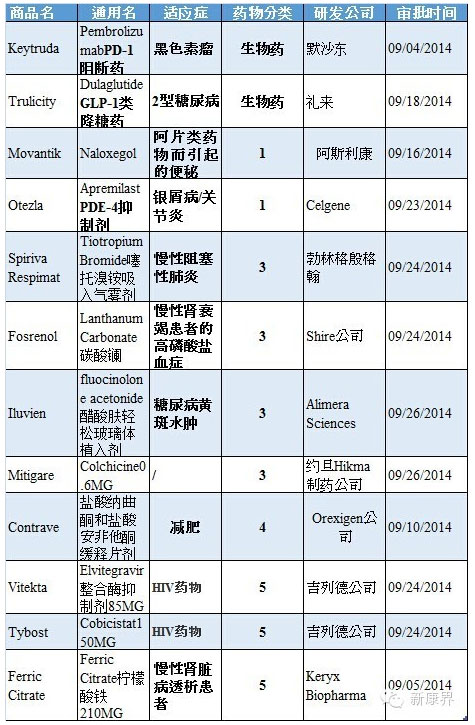
注:数据来源:根据FDA网站统计整理
药物分类:1类新分子实体;3类新剂型;4类新组合物;5类药物新规格或新生商;6类新适应症
黑色素瘤生物药Pembrolizumab
2014年09月04日美国FDA审批默沙东公司研发的黑色素瘤生物药Pembrolizumab(商品名Keytruda)上市。1类新分子实体药物2个,2013年Pembrolizumab在美国被授予突破性治疗药物资格用于晚期恶性黑色素瘤的治疗。Pembrolizumab在日本孤儿药也被授予孤儿药资格用于恶性黑色素瘤的治疗。